Entrada destacada
Los Trece de la Fama.
Esta es la segunda parte del Blog " Paracelso tenía razón" http://drlopezcorbalan.blogspot.com/ Como decía Fray Luis de León...

Mostrando entradas con la etiqueta COVID-19. Mostrar todas las entradas
Mostrando entradas con la etiqueta COVID-19. Mostrar todas las entradas
miércoles, 19 de mayo de 2021
Los despropósitos de Astra Zeneca. NO SE PUEDE HACER PEOR.
Lo mínimo que se le puede pedir a un Minsitro de Sanidad es que sea SANITARIO, que sepa de lo que trata su Ministerio.
NO PUEDEN IRSE DE ROSITAS LOS NEGLIGENTES Y CRIMINALES.
No tiene mucho sentido nombrar Ministro de Ingenieria Hidráulica a un señor que no es ingeniero. Por ejemplo.
En España tenemos una larga tradición de Ministros de Sanidad que no tienen ni la más remota formación sanitaria.
Así nos va.
El ministro patibulario de la triste figura, ese Ministro filósofo con cara de empleado de pompas fúnebres, Illa. Tiene en el debe 125.000 muertos. Ha gestionado con el culo esta crisis sanitaria,la peor de nuestra Patria en los últimos 100 años. Un completo fracaso. Un desastre sin paliativos. Gente muriendo colgada de los telefonos 900 esperando una ayuda que nunca llegó. Ancianos muriendo a cascoporro mientras la señora Dalias, si, la nueva minsitra, daba saltitos debajo de una pancarta mientras el virus se extendía inmisericorde.
Y ahora, para completar las zafias e indecentes gestiones de NEGAR LA UTILIDAD DE LAS MASCARILLAS ( día 26 de febrero del 2020, que me acuerdo muy bien), además de negar la gravedad de la crisis, ademas de comprar test inadecuados, sin ningna calidad, importados desde China sin las más mínimas garantías, pues a hora la terminan de arreglar con la pésima gestión de esta vacuna ChAdOx de Astra Zeneca.
El despropósito , la ineficacia, el desastre farmacológico, la apatía, la abulia, la incompetencia, la estupidez palmaria de la señora orquídeas ( o Vileta, u Ordalias, o Dalias) o como se llame.
Es realmente dificil entender este lio monumental que ha montado este caótico Ministerio de Sanidad lamentable.
NO HAY NINGUNA RAZON FARMACOLOGICA QUE JUSTIFIQUE ESTE DESASTRE DE NO PONER LA VACUNA ASTRA´ZENECA A LOS 2,2 MILLONES DE PERSONAS QUE ESPERAN LA SEGUNDA DOSIS COMO AGUA DE MAYO PARA ESTAR ADECUADAMENTE INMUNIZADOS.
Pero además es que esto supone saltarse los protolos que se han hecho para la aceptación de ésta vacuna por parte de la Agencia Europea del Medicamento, que dejan palmariamente claro que hace falta un "booster" o segunda dosis de recuerdo, que ademas no debe de retardarse mas de 9-12 semanas, en el peor de los casos.
Cuandos e infecten ( y mueran) cientos de personas que solo tienen puesta la primera dosis de asta zeneca, y que por lo tanto NO ESTAN INMUNIZADAS. ¿QUIEN VA A PAGAR ESAS MUERTES POR NEGLIGENCIA E IRRESPONSABILIDAD
NO PUEDEN IRSE DE ROSITAS LOS NEGLIGENTES Y CRIMINALES. 125.000 MUERTES ( EXCESO DE MUERTES, YA SABEN ESO QUE EL 90 POR CIENTO SON VICTIMAS DE COVID 19.
Etiquetas:
COVID-19,
CRIMINAL,
NEGLIGENCIA,
pandemia,
SANIDAD
viernes, 30 de abril de 2021
Diseño de fármacos antivirales usando modelos de supercomputacion y docking.
Estimad@ autor@:
Es un placer comunicarle que el trabajo de su autoría: "Diseño de medicamentos anti COVID19 in silicio (Mpro)" ha sido publicado e incluído en el último número de la Revista Electrónica de PortalesMedicos.com:
Diseño de medicamentos anti COVID19 in silicio (Mpro)
Autor principal: Juan Carlos López Corbalán
Vol. XVI; nº 8; 452
Designing Drugs targeting Mpro of SARs-CoV2 in silicio
Fecha de recepción: 03/02/2021
Fecha de aceptación: 19/04/2021
Incluido en Revista Electrónica de PortalesMedicos.com Volumen XVI. Número 8 – Segunda quincena de Abril de 2021 – Página inicial: Vol. XVI; nº 8; 452
Autores:
Juan Carlos López Corbalán, José Miguel Seguí Ripoll.
Administración general del estado; Hospital San Juan de Alicante. Alicante, España.
Resumen:
En la actualidad la pandemia de la beta coronavirus SARS-CoV2 ha causado más de 2,2 millones de muertos y 120 millones de infectados, y las cifras quedarán obsoletas en pocos minutos, porque están muriendo entre 19.000 y 26.000 personas al día en el planeta.
De momento no hay un tratamiento antiviral efectivo contra esta plaga. Creemos que el diseño de fármacos por súper computación podría ser una útil herramienta para encontrar ése antiviral barato, efectivo, por vía oral y sin reacciones adversas. Se estudian los fármacos que actúan sobre la proteasa Mpro del SARS-CoV-2 y los que actúan sobre la RNA dependiente RNA polimerasa dependiente de RNA. “RdRp”
Palabras clave: COVID-19, in silicio, medicamentos, antivirales, diseño
Abstract:
Currently the pandemic of the beta coronavirus SARS-CoV2 has caused more than 2.2 million deaths and 120 million infected, and among 19,000 and 26,000 people are dead every day.
At the moment there is no effective antiviral treatment against this disease. We believe that the docking of drugs by supercomputation could be a useful tool to find that antivirals. Drugs that act on the SARS-CoV-2 protease Mpro and those that act on RNA-dependent RNA polymerase are reviewed in this paper.
Keywords: COVID-19, in silicio, drugs, antivirals, design, RdRp, Mpro.
Los autores de este manuscrito declaran que:
Todos ellos han participado en su elaboración y no tienen conflictos de intereses. La investigación se ha realizado siguiendo las Pautas éticas internacionales para la investigación relacionada con la salud con seres humanos elaboradas por el Consejo de Organizaciones Internacionales de las Ciencias Médicas (CIOMS) en colaboración con la Organización Mundial de la Salud (OMS) https://cioms.ch/publications/product/pautas-eticas-internacionales-para-la-investigacion-relacionada-con-la-salud-con-seres-humanos/
INTRODUCCION.
A día de hoy no hay un antiviral eficaz para tratar la COVID19. El único fármaco que ha logrado disminuir la mortalidad (de forma estadísticamente significativa) es la Dexametasona, que no es propiamente un fármaco antiviral, sino un corticoide inhibidor de las reacciones antiinflamatorias.
La pandemia actual de COVID-19 cuyo agente etiológico es el SARS-CoV-2 es responsable de la emergencia sanitaria mundial.
Hay un principio básico en Virología que siguen TODOS los virus de la clasificación de Baltimore (que es el nombre del Científico David Baltimore) Premio Nobel Medicina, 1977) que la realizó.
Ese axioma fundamental dice:
Todos los virus del planeta siguen la regla de que para generar sus genomas tienen que hacer RNA mensajero y ser leído por los ribosomas del huésped. TODOS.
Fig.1 Axioma de la Virología.
Por lo tanto, los fármacos antivirales podrán tener diferentes “targets”, pero todos al final pasan por esas horcas caudinas de tener que traducir su m RNA en proteínas o material genómico usando las organelas, ribosomas y enzimas del huésped a quien infectan.
Actualmente, no existe un remedio específico disponible contra el SARS-CoV-2.
En consecuencia, es fundamental desarrollar un antiviral efectivo, barato, de administración oral, de buena biodisponibilidad, de toxicidad selectiva y además barato.
Hay 28 proteínas sobre la superficie del virus, pero las 4 más conocidas son:
La proteína S (espiga), la N (nucleocápside), la M (de membrana) y la E (Envoltura).
En la actualidad casi todo el esfuerzo de focaliza sobre los 1274 aminoácidos de la proteína S o espícula. Al ser grandes estructuras, podemos visualizarlas por técnicas de Crio EM y VR y buscar esos residuos hidrofóbicos formados por aminoácidos aromáticos (“pockets”) donde podrían encontrarse receptores para moléculas de peso molecular de entre 350 y 900.
Las dianas terapéuticas más adecuadas las buscaremos apoyándonos en la supercomputación y el docking y cribaje de nuevas moléculas o reposicionamiento de otros fármacos ya aceptados y autorizados para tratar otras patologías y orientarlo para atacar las dianas terapéuticas del SARS-CoV-2 (12).
¿Son útiles los diseños de fármacos por ordenador? Pues sí. Los súper ordenadores no diseñan nada, no crean nada si no están bien programados para ello, pero son muy útiles como herramienta accesoria y ponemos dos ejemplos.
Fig. 2 El Zanamavir (Relenza ®), diseñado con métodos computacionales contra el receptor siálico del ortomixovirus.
O el Indinavir, Crixivan ®, dirigido hacía la proteasa del retrovirus HIV.
Son dos ejemplos válidos para sustentar que se pueden diseñar fármacos antivirales con la ayuda de las técnicas de docking, cribado y uso de supercomputación para el screening “in silicio” de nuevos fármacos anti virales.
Innecesario decir que no se ha encontrado hasta el momento ningún fármaco antiviral contra el SARS-CoV2 (2). No es fácil. Y la historia nos demuestra que algunos antivirales se descubrieron i por serendipia, como la Amantadina, que mejoró los síntomas gripales de un grupo de enfermos a los que se trataba buscando antihistamínicos. O las muy conocidas de Pfizer, el Sildenafilo (Viagra) ®, originalmente se buscaba como antihipertensivo.
Lo anteriormente expuesto nos obliga a reconsiderar que esta pandemia hace que cambie el paradigma y se usan las supercomputadoras y los programas de diseños y desarrollo de fármacos por métodos computacionales “in silicio”. E incluso se hace una modificación de la teoría heurística del docking y se realiza cribado selectivo sobre fármacos ya aprobados, de forma y manera tal que podamos “ganar tiempo” y podamos encontrar ésa solución farmacológica de la pandemia. Tal sería el caso del Raloxifeno, fármaco ya autorizado que ahora se demuestra que por cálculo químico farmacéutico tiene acción inhibitoria de la RNA polimerasa del SAR-CoV 2. Puntualizar que esto es una ayuda a la investigación, pero los supercomputadores no “diseñan” fármacos sólo, sino tan solo una herramienta accesoria, no son necesariamente predictivos.
Y quizás lo más importante: El “docking” no demuestra que la molécula se una efectivamente al receptor.
Docking o acoplamiento molecular computarizado (1)
Virtual screenig o identificación y búsqueda de compuestos dentro de una colección o conjunto de similares (un a library previa) y características. Mediante hits computacionales vamos experimentando. Un ejemplo en estudios de Farmacognosia nos ponemos a identificar todos los alcaloides del cornezuelo del centeno (Claviceps purpúrea, que parasita al centeno (Secale cereale). Esto es el cribado virtual, usando supercomputación o modelo “in silico”. Incrementamos la probabilidad de encontrar moléculas activas.
Pharmacophore modeling el fin es detectar el arreglo tridimensional de las características mínimas en forma de mapeo de la nube electrónica y, abajo se ilustra el modelo farmacóforo en el que se presentan las interacciones con el receptor. La esfera roja de elevada carga negativa ( -2,19) y – 11,74, aceptan puentes de hidrógeno, los anillos en azul dan y el anillo Fig.4 Farmacoforos.significa que puede tener nube electrónica pi, como el benceno
En la figura 5 de abajo tenemos el ácido trimetil aurin tricarboxílico, con sus tres grupos farmacóforos marcados con un asterisco.
Dianas terapéuticas para el SARS-CoV-2
La RNA polimerasa. Ejemplo: Remdesivir, o Metisazona (3), por poli farmacología: Raloxifeno.
poli farmacología: tenemos ya otras moléculas aceptadas, pero con otra indicación terapéutica, con lo cual podemos usarlos para una nueva indicación sin volver a tener que realizar estudios toxicológicos.
La eEF1A (Eukaryotic translation elongation factor 1 alpha), en éste caso realmente no actuamos sobre el virus, sino sobre un factor del huésped, pero lo hemos incluido igualmente. Ej.: Plitidepsina. Otro ejemplo de cribado en library. Este fármaco se usaba contra el mieloma múltiple. Ahora se le busca aplicación en Fase I contra la Covid 19.
La MPro o Proteasa 3CLpro.La estructura de la Mpro la tienen en la Fig. 6 Ejemplos serían el Ebselen también llamado PZ51 DR3305, ó SPI-1005, Carfilzomib (7,8,9).
Nos vamos a centrar en ésta Mpro, usando técnicas de cálculo químico farmacéutico buscando moléculas de peso molecular entre 340 y 900 que se unan a esos residuos hidrofóbicos que se forman en determinadas regiones y probar a base de “fuerza bruta” diversos fármacos que han demostrado actividad sobre Mpro son Etopósido, Hesperidina, Velpatasvir, Diosmina y Venetotoclax.
Fig.7.
La RnRp ó Ribonucleasa dependiente de m RNA polimerasa (4). Se descubrieron partir de estudios sobre el Mengovirus y el virus de la polimielitis cuando se observó que estos virus eran insensibles a la actinomicina D, un fármaco que inhibe la síntesis de ARN celular catalizada por ADN. Esta falta de sensibilidad sugirió que existe una enzima específica del virus una enzima propia de los virus de ARN que cataliza la replicación del ARN a partir de una plantilla de ARN. que podría copiar ARN de una plantilla de ARN y no de una plantilla de ADN.
Como el MK-7376, al parecer tienen acciones como inhibidores de la proteína ácida con función endonucleasa o los dos compuestos CoViTris2020 and ChloViD2020 (5) ó el Mr224 (14)
Los canales ionóforos: Ej.: Ivermectina al 0,6 %. Esta acción “in vitro se está estudiando también “in vivo” en ensayos clínicos.
Los inhibidores de la proteasa alfa ceto glutarasa. Ej.: Telaprevir, Borceprevir. Estos fármacos inhiben la proteasa del virus de la Hepatitis C, en concreto su IP de serina NS3-4A del VHC, enzima esencial para la replicación del virus. Dudoso que tengan ninguna acción contra el SARS-CoV-2, aunque ambos sean virus RNA mono catenarios de la clasificación IV de Baltimore.
Elevación de pH endoplásmico, inhibiendo metabolismo viral: Hidroxicloroquina.
Hablar dela Cloroquina y su hidroxiderivado nos llevaría al escándalo Surgisphere y la revista The Lancet, y preferimos dejarlo de lado. La Cloroquina tiene varios mecanismos de sobre el SARS-CoV-2, impidiendo su entrada y difusión a la célula, pero el aumento del Ph intracelular es quizás el más importante.
Inhibidores de la Fusión. Que inhiben los procesos de anclaje y fusión. En concreto a la proteína TMPRSS2.
Aquí tendríamos el Acetato de Camustat, del cual se están haciendo ensayos clínicos. Fármacos que inhiben los procesos de anclaje y fusión. En concreto a la proteína TMPRSS2.
Cuando el virus SARS-CoV2 se ancla al receptor ACE/2 h de las células epiteliales, sufre dos cleavages.
1) Uno es dependiente de furinas, una proteína existente en el propio sistema del huésped, pero que el virus, ladinamente usa contra el huésped (el hospedador, como lo llaman en los libros de Virología sudamericano), lo que hace para aprovecharse de nuestro sistema para empezar a generar virones meta estables anclarse (S1) y luego fusionarse (S2).
Estos son pasos muy importantes sobre los que conviene profundizar, como haremos más adelante.
2) El segundo cleavage se produce con la S2 cambiando la conformación y aparece una proteína de fusión, absolutamente necesaria para penetrar en la célula epitelial humana que es el huésped (no se ha demostrado la posibilidad en células endoteliales, como proponían dos cirujanos torácicos americanos.
Hay un cambio conformacional y pasamos de una proteína pre fusión PDB-6VSB a otra proteína de post fusión. PDB:6LXT.
Aquí actúa el Mesilato de Camustat, inhibiendo la TMPRSS2 y sobre el que se están haciendo ensayos clínicos que determinen su uso en clínica. Esta proteína de fusión del virus es fundamental, junto con el de anclaje.
¿Cuándo se produce el “cleavage”?
¿En la superficie de la célula o en el endoplasma?
¿Ese proceso de cambio conformacional va influenciado por el pH?
Un pH muy básico (conseguido por ejemplo tomando HCQ, subiendo el pH intracelular por encima de 8,5 inhibirían los procesos endonucleares del virus, produciendo su enlentecimiento reproductivo e inhibe el proceso
El “cleavage” (anglicismo para definir rotura enzimática) de S1 y S2 se realiza por la llamada a proteína de corte de furinas. Si, las mismas proteínas de corte de furinas que, según la disidente china son una de las tres características del virus propias de haberse sintetizado en un laboratorio, a partir de dos virus corona del resfriado vulgar y luego una insertación de la espícula por técnicas que habrían llevado unos seis meses. Eso explicaría también las notables diferencias entre las tres proteínas de la espiga de murciélago de herradura, pangolín ( Manus javanica) y SARS-CoV 2.
9. Mecanismo poco conocido. Inducción de errores por parte de la proof reading del virus, posiblemente por ser análogo de citosina. En éste cajón de sastre tendríamos al MK 4284 o Molnupiravir.
10. Otros. Aclarubicin, TMC-310911 y Faldaprevir (13), posibles inhibidores de Mpro.
NO hemos incluido en ésta revisión los siguientes grupos:
1 Los anticuerpos monoclonales, porque su mecanismo de acción va ligado a los epítopos o determinantes antigénicos. Dejamos fuera al Lyco 5555 ®, el Regeneron ® ó el anticuerpo monoclonal ya “clásico” contra el SARS-CoV-1, el CR 3022 S.
2 los inhibidores de Il6: Tocilizumab y Siltuximab. Porque no son fármacos específicos para la COVID19, ya se usaban para otras patologías y ya estaban aprobados y no hay que volver a hacer estudios de toxicidad crónica y agua, pues ya están en su Ficha Técnica.
Por la misma razón, dejamos fuera de este estudio al Sarilumab, Bariticinip , Erlitinib, y Sumatinib.
3 Los inhibidores de la IL -1. El Anakinra. Mismo motivo.
4 Inhibidores JAK 1 y JAK 2: Ruxolitinib
5 El plasma humano de enfermos convalecientes, porque hay dudas sobre su efectividad y además aumentan los accidentes trombóticos dada la elevada reología del plasma de convalecientes.
MATERIAL Y METODOS.
Primeramente se hizo una búsqueda bibliográfica primaria de la información obtenida de clinicaltrials.gov que está gestionada por la National Library of Medicine (NLM) y el National Institutes of Health (NIH) de la Food and Drug Administration del Gobierno de los Estados Unidos de América.
Igualmente se han utilizado los buscadores médicos y las revistas BioXriv, ChemXriv, New England Journal of medicina y JAMA.
Se han excluido los artículos de The Lancet porque, después del escándalo Surgiphere, no nos merece confianza ni credibilidad la citada revista.
Luego se emplearon técnicas de Vr empleando un sistema Oculus Quest 2 white, bajo licencia de Nanome Inc. soportada en un modelo de PC con microprocesador MSi Trident 3 10 SI-016EU 17-10700/16/512/GTX 1660 SA/W.
Hay otros porgramas, como el Link3D o el Naive Bayes(12). Algoritmo Básico del que se dice (12) tiene una eficacia del 73% para predecir medicamentos con actividad anti SARS-CoV-2.
RESULTADOS:
Hay 28 proteínas en la superficie del betacoronavirus causante de la COVID19, pero nos hemos centrado en los fármacos que inhiben la proteasa M pro del coronavirus (CoV) (Mpro también llamada 3CLpro), que juega un papel indispensable en el ciclo biológico del virus.
Aquí ven la serie de cinco moléculas que se unen a los residuos hidrofóbicos (“bolsillos o pockets”). En la figura de abajo ven los citados residuos hidrófobos marcados en negro. Usando técnicas de docking y su afinidad química entre sustrato y receptor expresadas kcal/ mol.
Otros autores (16) han usado El llamado Glide-Schodinger dock score, así se descubrieron como inhibidores de la Mpro el Lopinavir, Amodiaquina, y el Digalato de teaflavina.
Fig. 9 Pocket 1 Energía: -8,41 kcal/mol.
Fig. 10 Pocket 2. Energía: -7,77 Kcal/mol.
Fig. 11 Pocket número 3 : Energía: -8,51 Kcal/mo
Fig. 12 Pocket número 4.: Energía: -8,29 kcal/mol.
De origen farmacognósico nos encontramos otros productos. (6) La épsilon –Viniferina ( -8,6 kcal/mol) o el Dehirdectol ( -10,3 kcal/mol), el Carnosol ( -8,2 kcal/mol) el Arjunglucoside ( -7,78 kcal/mol) y el Rosmanol (- 7,95 kcal/mol). (10)
Esta revisión prevé que los inhibidores dirigidos a CoV Mpros podrían convertirse en fármacos antivirales de amplio espectro en caso de COVID-19 y otras enfermedades relacionadas con CoV (proyecto Excakate4Covid). Los resultados de la estructura cristalina y del acoplamiento han demostrado que los inhibidores de Ebselen, TDZD-8 y derivados de α-cetoamida. Fig. 13. como potenciales fármacos, ya que, en el laboratorio buscamos el concepto de Mutación letal y entrada en catástrofes de error, que podría conseguirse con la aplicación de varios de éstos compuestos en asociación, con lo que podriamos disminuir su toxicidad.
La inducimos cuando nos dedicamos a ir exponiendo al virus a diversos antivirales que actúan sobre diferentes mecanismos, aumentando la tasa de error en la RNA polimerasa del virus de forma artificial hasta que se extingue el virus. Aquí podría ser una asociación de inhibidor de la proteasa, un inhibidor de la polmerasa y un inhibidor de la proteína de fusión.
Otros farmacos que también tienen el mecanismo conjunto de la entrada en catástrofe de error son el Favipiravir, en estudios realizados en Japón, la Ribavirina o la Ivermectina al 0,6 % , cuyo mecanismo de acción sería bloquear los los canales ionóforos del virus.
Los genomas de los viriones metaestables tienen que hacer mRNA, que tendrá que ser leído por los ribosomas del huésped para poder ser leídos por los ribosomas.
CONCLUSIONES
El diseño de fármacos anti COVID19 por técnicas de cribaje, acoplamiento molecular computarizado y modificación de los farmacóforos puede ser una buena herramienta terapéutica para encontrar nuevos antivirales.
En la actualidad hay varios fármacos anti COVID19, especialmente inhibiendo la proteasa del virus ( 11) , pero de momento no hay tratamiento de la enfermedad.
El único medicamento que ha demostrado disminuir la mortalidad de forma estadísticamente significativa es la Dexametasona, pero no es en si un fármaco antiviral, sino un modificador de la respuesta inflamatoria.
Los compuestos Ivermectina al 0,6 % ( inhibidor de los canaes), la Amilorida ( proteína E), Remdesivir ( inhibidor de la RNA polimerasa) y MK 4482 son interesantes alternativas, pero ningno de ellos ha demostrado ser la panacea que todos esperamos para curar esta enfermedad.
Virtual screenig o identificación y búsqueda de compuestos dentro de una colección o conjunto de similares (un a library previa) y características. Mediante hits computacionales vamos experimentando. Un ejemplo en estudios de Farmacognosia nos ponemos a identificar todos los alcaloides del cornezuelo del centeno (Claviceps purpúrea, que parasita al centeno (Secale cereale). Esto es el cribado virtual, usando supercomputación o modelo “in silico”. Incrementamos la probabilidad de encontrar moléculas activas.
En cuanto al origen de la epidemia, no es el objetivo del trabajo sumergirse en esas complejidades, pero, cualquier científico que pretenda llevar a cabo una cruzada contra la hipótesis de la zoonosis basándose en que a día de hoy no se ha encontrado al paciente 0, ni conocemos al vector intermediario va por un mal camino. Ningún científico que vaya contra el dogma oficial nunca obtendrá ni fondos, ni subvenciones, ni podrá publicar nada. Y se le cerrarán todas las puertas. Y seguimos pensando que , esa teoría especulativa de la disidente china tiene un talón de Aquiles: dice que el coronavirus de murciélago R aTGa 13 que tiene un genoma idéntico al 96,1 % con el wild type que produce la COVID19 y se secuenció el 10 de Enero del 2020, no existe en la naturaleza y es un virus artificial creado por el Ejército Chino. Pero no da más detalles, no dice que fue aislado y anunciado en journals y paper en 2013 y ella se ha esperado 7 años antes de decir que es falso. No convence y parece más plausible la vía de que ésta pandemia es una zoonosis.
Por una simple cuestión estadística. Hay 10 elevado a 30 virus en un mililitro de agua de mar cerca de una depuradora. Se calcula que la biomasa de todos los virus del planeta es de 10 elevado a la 48. En la fauna silvestre circulan en torno a 1,6 millones de virus distintos, y entre 631 000 y 827 000 de ellos podrían ser zoonóticos. Existen muchísimos virus que nunca han sido aislados, pero que por fuerza en próximos años podrán volver de nuevo con la misma o peor fuerza que tiene éste actual.
Ahora imaginen que la próxima pandemia, en vez de tener una letalidad como la del SARs-CoV-2 baja, del 2-3 %, nos encontremos una mutación con una letalidad como el arenavirus de la fiebre Lhasa ó el de la fiebre hemorrágica Marburg.
Quizás dentro de unos años sepamos más. Para la llamada “Gripe española” hubo que esperar 15 años para descubrir, analizando unas muestras de cadáveres conservados en pendregast, que en 1932 se encontró y aisló el verdadero agente de la pandemia de 1918-20-
Esperemos que no tengan que pasar 15 años para saber el origen de ésta pandemia.
Esperemos que las técnicas de docking nos permitan encontrar un antiviral específico contra el SARS-CoV-2, esa “bala mágica” que decía Ehrlich que tendrá que pasar, absolutamente, sobre el M RNA viral que es leído por los ribosomas 80 S de la especie humana.
BIBLIOGRAFIA-
(1) José L.Medina-Franco Jl, Fernández-de Gortaria E, Naveja J.Avances en el diseño de fármacos asistido por computadora. Progress in computer-aided drug design. Educación Química; 2015 26, (3) 180-186.
(2) Cava C, Bertoli G, Castiglioni I. In Silico Discovery of Candidate Drugs against Covid-19. Viruses. 2020 Apr 6;12(4):404. doi: 10.3390/v12040404. PMID: 32268515; PMCID: PMC7232366.
(3) Shah B, Modi P, Sagar SR. In silico studies on therapeutic agents for COVID-19: Drug repurposing approach. Life Sci. 2020;252:117652. doi:10.1016/j.lfs.2020.117652
(4) Koonin, E.V., Gorbalenya, A.E. and Chumakov, K.M.(1989), Tentative identification of RNA-dependent RNA polymerases of dsRNA viruses and their relationship to positive strand RNA viral polymerases, FEBS Letters, 252, doi: 10.1016/0014-5793(89)80886-5
(5) Rabie AM. CoViTris2020 and ChloViD2020: a striking new hope in COVID-19 therapy. Mol Divers. 2021 Jan 3:1–16. doi: 10.1007/s11030-020-10169-0. Epub ahead of print. PMID: 33389560; PMCID: PMC7778709.
(6) Shah B, Modi P, Sagar SR. In silico studies on therapeutic agents for COVID-19: Drug repurposing approach. Life Sci. 2020;252:117652. doi:10.1016/j.lfs.2020.117652
(7) Shah B, Modi P, Sagar SR. In silico studies on therapeutic agents for COVID-19: Drug repurposing approach. Life Sci. 2020;252:117652. doi:10.1016/j.lfs.2020.117652
(8) Alnajjar R, Mostafa A, Kandeil A, Al-Karmalawy AA. Molecular docking, molecular dynamics, and in vitro studies reveal the potential of angiotensin II receptor blockers to inhibit the COVID-19 main protease. Heliyon. 2020 Dec;6(12):e05641. doi: 10.1016/j.heliyon.2020.e05641. Epub 2020 Dec 3. PMID: 33294721; PMCID: PMC7713577.
(9) Wu J , Wang H , Li B . Structure-aided ACEI-capped remdesivir-loaded novel PLGA nanoparticles: toward a computational simulation design for anti-SARS-CoV-2 therapy. Phys Chem Chem Phys. 2020 Dec 23;22(48):28434-28439. doi: 10.1039/d0cp04389c. PMID: 33305304.
(10) Keretsu, S., Bhujbal, S.P. & Cho, S.J. Rational approach toward COVID-19 main protease inhibitors via molecular docking, molecular dynamics simulation and free energy calculation. Sci Rep 10, 17716 (2020). https://doi.org/10.1038/s41598-020-74468-0
(11) Zhenming Jin, Xiaoyu Du, Yechun Xu, Yongqiang Deng, Meiqin Liu, Yao Zhao, Bing Zhang, Xiaofeng Li, Leike Zhang, Yinkai Duan, Jing Yu, Lin Wang, Kailin Yang, Fengjiang Liu, Tian You, Xiaoce Liu, Xiuna Yang, Fang Bai, Hong Liu, Xiang Liu, Luke W. Guddat, Gengfu Xiao, Chengfeng Qin, Zhengli Shi, Hualiang Jiang, Zihe Rao, Haitao Yang
bioRxiv 2020.02.26.964882; doi: https://doi.org/10.1101/2020.02.26.964882
(12) Mohapatra S, Nath P, Chatterjee M, Das N, Kalita D, et al. (2020) Repurposing therapeutics for COVID-19: Rapid prediction of commercially available drugs through machine learning and docking. PLOS ONE 15(11): e0241543. https://doi.org/10.1371/journal.pone.0241543
(13) Mohapatra S, Nath P, Chatterjee M, Das N, Kalita D, et al. (2020) Repurposing therapeutics for COVID-19: Rapid prediction of commercially available drugs through machine learning and docking. PLOS ONE 15(11): e0241543. https://doi.org/10.1371/journal.pone.0241543
(14) El Hassab Mahmoud A., Shoun Aly A., Al-Rashood T., Al-Warhi Tarfah, Identification of a New Potential SARS-COV-2 RNA-Dependent RNA Polymerase Inhibitor via Combining Fragment-Based Drug Design, Docking, Molecular Dynamics, and MM-PBSA Calculations JFrontiers in Chemistry.2020; 8:915-916. DOI=10.3389/fchem.2020.584894
(15) K. Abraham Peele, Chandrasai Potla Durthi, T. Srihansa, S. Krupanidhi, Vijaya Sai Ayyagari, D. John Babu, M. Indira, A. Ranganadha Reddy, T.C. Venkateswarulu,Molecular docking and dynamic simulations for antiviral compounds against SARS-CoV-2: A computational study,Informatics in Medicine Unlocked; 2020,(19)100-345ISSN 2352-9148,https://doi.org/10.1016/j.imu.2020.100345.
Etiquetas:
antivirales,
COVID-19,
diseño,
docking,
farmacos,
supercomputacion
miércoles, 31 de marzo de 2021
Publicacion Revista Portales Médicos: Acción sinérgica de Camostat e Hidroxicloroquina.
EN EL SIGUIENTE ARTICULO SE PLANETA EL TRATAMIENTO COMBINADO DE LA covid19 EMPLEANDO DOS FARMACOS DIFERENTES QUE ACTUAN EN EL PROCESO DE ENTRADA DEL VIRUS AL ORGANISMO.
Creemos que es un trabajo que esta basado en solidos principios de interaccion de la HCQ con las catepsinas del endosoma y el Mesilato de camostat como inhibidor de la TMPRSS2 en la superficie de la membrana y , al menos heurIsticamente, propone de forma cristalina y explicita este mecanismo de actuacion.
Publicado en Portales.Medicos.Com.
https://www.revista-portalesmedicos.com/revista-medica/sinergia-de-potenciacion-farmacologica-anti-covid-19-mesilato-de-camustat-e-hidroxicloroquina/
Hace unos meses le preguntaron al Ministro sepulturero, Illa, maravilla; que qué era la Cloroquina. pROBABLEMENTE TODAVIA NO SABE LOQ UE ES LO QUE LE PREGUNTARON.
El entonces Ministro de Sanidad del Reino de España se quedó con esa cara de empleado de pompas fúnebres, con esa cara de ausencia de actividad bioeléctrica en el cerebro y dijo que " ya lo consultaria" y se fue vergonzosamente de la Sala de Prensa sin contestar a la pregunta. Básicamente, porque no tenía IDEA de lo que es la Cloroquina.
Un ejemplo mas de que tenemos los PEORES POLITICOS EN EL PEOR MOMENTO POSIBLE.
Esta bitácora no es politica, porque la Política es una ciénaga, una charca mefítica , un lupanar donde pululan palanganeros con su cubilete de permanganato limpiando glandes ajenos, un médico ( que no doctor) que se ha pasado al " lado oscuro", vendiéndose por 4450 euros al mes, que es lo que cobra por gestionar esta pandemia con criterios políticos, no sanitarios.
Aquí tirnen la publicación realizada sobre la acción sinérgica del Mesilato de Camostat y la Hidroxicloroquina, que creemos aporta un interesante nuevo punto de vista sobre el abordaje terapéutico de ésta terrible pandemia.
Etiquetas:
Camostat,
COVID-19,
Hidroxicloroquina,
pandemia
domingo, 7 de febrero de 2021
Los cleavages. Modulacion de la entrada del Virus SARS CoV2 en la célula humana. EL PUNTO CLAVE. ( SCHWERPUNKTE).
Aproximaciones farmacológicas al tratamiento del SARS-Cov2.
En la superficie del virus hay 28 proteínas, la más conocida y estudiada, los 1273 aminoácidos de la Spike protein.
Hay entre 15 y 45 espículas en la superficie del virus. InClinadas formando un ángulo de 40 grados.
El virus es monocatenario RNA, strand (+), de 100-120 nm.
La subunidad S1 se encarga del anclaje al receptor humano ACE/2 y la S2, se encarga de la fusión.
Hay dos procesos claves, dos "cleavages".
a) Cleavage de la subunidd S1/ S2, realizado por proteínas de corte de furina.
Si, las mismas que la disidente china dice que son la clave para demostrar ,o que los Journals de Ciencia le han negado, que es una entelequia de laboratorio ( no está aceptado por la comunidad científica.
Este cleavaje no es imprescindible para la infecciosidad del virus, pero
b) Cleavage S2 prime ( la proteína TMPRSS", su inhibidor posible fármaco es el Mesilato de Camustat). Este paso lo hacen todos los coronavirus.
Esa proteína de fusión tienen nombre. Se puede producir esos cambios conformacionales, pero el paso final ES NECESARIO EL SEGUNDO CLEAVAJE. Libera el peptido de fusión.
Algunos alfa coronavirus no tienen éste sitio de acción de la proteasa, pero si los beta coronavirus.
Es en éste proceso donde aparece la llamada proteína de Fusión. No confundir proteina de PRE fusión ( 6VSB) con la proteína POST Fusión ( 6LXT) . UN mecanismo bastante similar al del Virus Respiratorio sincitial ( llamada proteína F).
Farmacológicamente sería interesante un ensayo clínico asociando un fármaco inhibidor de la TMPRSS2 ( Mesilato de Camustat), con fármacos capaces de aumentar el pH endoplásmico,( si, la famosa Hidroxicloroquina). Sabemos que un aumento del pH endoplásmico por encima de 8,4 inhibe el metabolismo del virus. Quizás poco específico, pero lo inhibe.
Después del escándalo Surgisphere y las implicacones politicas, difícil que vuelvan a hacerse ensayos clínicos sobre HCQ.
martes, 17 de noviembre de 2020
Estado actual de las vacunas y Ensayos Clínicos .
Actualizar conocimientos. La carrera por las vacunas ha comenzado.
En los enlaces adjuntos vemos la evolución a tiempo real de la pandemia, así como el estado actual de las investigaciones clínicas.
Etiquetas:
actualización,
ciencia,
COVID-19,
estacionalidad,
hopkins,
jonh,
pandemia,
twiv,
vaccines,
vacunas
sábado, 2 de mayo de 2020
Amantadina como agente lisosomotrópico contra el COVID19.
doi: https://doi.org/10.1101/2020.04.05.026187
Fórmula del compuesto, que ya se utilizó como antiparkinsoniano hace treinta años, recuerdo haberloe studiado como un gran fármaco en Farmacia Galénica II como una "gran esperanza" para la "parálisis agigante", esa enfermedad neurológica .
Hoy día está bastante aparcado y poco utilizado en Neurología.
.

Fórmula del compuesto, que ya se utilizó como antiparkinsoniano hace treinta años, recuerdo haberloe studiado como un gran fármaco en Farmacia Galénica II como una "gran esperanza" para la "parálisis agigante", esa enfermedad neurológica .
Hoy día está bastante aparcado y poco utilizado en Neurología.
Se ha utilizado como antigripal, porque tiene acción virudicida contra los ortomixovirus, desde 1968.
Se conoce , pues, bastante bien. Se están intentando probar todo tipo de fármacos y , para evitar inumerables ensayos clínicos se prefiere probar algunos de los que ya se conocen sus efectos secundarios y no nos sorprende con alguna reacción inesperada.
.
El COVID19, muta al menos 1 vez al mes. Cosa " normal" , porque los virus están siempre mutando, es parte de su "filosofía" de vida ( suponiendo o considerandolos como seres vivos, lo cual nos mete en un jardín complicado. El siguiente paso serían los priones.

Se han identificado al menos entre 8 y 30 mutaciones del COVID 19. Con unas diferencias de comportamiento e infección muy diferentes.
Está droga podría producir una " down regulation" de la expresión CTSB.
OJO al abstract.
Amantadine in addition to downregulating CTSL appears to further disrupt lysosomal pathway, hence interfering with the capacity of the virus to replicate. It acts as a lysosomotropic agent altering the CTSL functional environment. We hypothesize that Amantadine could decrease the viral load in SARS-CoV-2 positive patients and as such it may serve as a potent therapeutic decreasing the replication and infectivity of the virus likely leading to better clinical outcomes. Clinical studies will be needed to examine the therapeutic utility of amantadine in COVID-19 infection.
Etiquetas:
agente,
amantadina,
Antiflu,
COVID-19,
CRISPR-Cas9,
mutacion,
secuenciación,
Tamiflu
domingo, 12 de abril de 2020
El COVID-19 , unión al receptor mediante su anclaje a la Spike protein.
DEDICATORIA: Para Amelia:
En un artículo ya histórico publicado en Nature y con la resolución a 2,5 Amstrong de la unión entre h ACE/2 y el SARS-CoV-2 en su dominio de union ( RBD),
vemos como hay una unión entre la hélice N del receptor para angiotensina y el virus ( eso se llama RBM) . Está representado con la flecha naranja.
. Y hay que distinguir entre lo que es RBD y RBM. No es lo mismo.RBD: es el Dominio union ( region binding dominium) ,es la parte del COVID19 que se une al receptor de la angiotensina humana ( h ACE/2),que lo tienen aquí en su estructura por crio EM.
que es bastante abundante en células epiteliales del pulmón y en otros parénquimas del cuerpo humano. Esto explicaría otros síntomas del virus, como las lesiones dermatológicas simulando excoriaciones en extremidades acras y la miocarditis o los fallos renales agudos. Estos últimos también se explicarían por la catarata de citokinas que provoca el SARS-CoV-2 o COVID19 en el cuerpo de la especie humana.
El RBM es otra cosa: es el motivo de unión al receptor. Es una parte más pequeña del COVID, que se une específicamente con una helice N terminal del hACE/2.
En un artículo ya histórico publicado en Nature y con la resolución a 2,5 Amstrong de la unión entre h ACE/2 y el SARS-CoV-2 en su dominio de union ( RBD),
vemos como hay una unión entre la hélice N del receptor para angiotensina y el virus ( eso se llama RBM) . Está representado con la flecha naranja.
. Y hay que distinguir entre lo que es RBD y RBM. No es lo mismo.RBD: es el Dominio union ( region binding dominium) ,es la parte del COVID19 que se une al receptor de la angiotensina humana ( h ACE/2),que lo tienen aquí en su estructura por crio EM.
que es bastante abundante en células epiteliales del pulmón y en otros parénquimas del cuerpo humano. Esto explicaría otros síntomas del virus, como las lesiones dermatológicas simulando excoriaciones en extremidades acras y la miocarditis o los fallos renales agudos. Estos últimos también se explicarían por la catarata de citokinas que provoca el SARS-CoV-2 o COVID19 en el cuerpo de la especie humana.
El RBM es otra cosa: es el motivo de unión al receptor. Es una parte más pequeña del COVID, que se une específicamente con una helice N terminal del hACE/2.
La comparación entre los complejos SARS-CoV RBD/hACE2 y SARS-CoV-2 RBD/hACE2 permite entender por qué es más infectiva COVID-19 que SARS.
La SARS-CoV-2 RBM forma un interfaz de unión más grande y con más contacto con hACE2 que SARS-CoV RBM; se ha intentado explicar por química farmacéutica , razonándose que una de las razones es que el puente salino entre SARS-CoV RBD y hACE2 es más débil que el de SARS-CoV-2 RBD y hACE2, pero más favorable energéticamente.
Además, la estructura cristalina del complejo también contiene glicanos acoplados a los cuatro sitios de hACE2 y el sitio de RBD. Esa es la excusa que los que defienden la etiologia de la mutación natural del virus desde el murciélago, con o sin pasar por un vector intermedio. Esta teoría es extremadamente discutible, al emnos a día de hoy. Hay una cientifica Judy Mikovits, que defiende que el virus es un arma biológica.
Volveremos sobre ésto.Da mucho juego. Eterna discusión entre Verschwörungtheorie y los que deefienden el caractere "natural" del virus por mutaciones interespecies o a través de un huésped intermedio.
El glicano acoplado a Asn90 de hACE2 forma un enlace de hidrógeno con Arg408 del núcleo de RBD; esta interacción se conserva entre SARS-CoV-2 y SARS-CoV.
Las diferencias estructurales entre las RBMs de SARS-CoV-2 y SARSCoV RBMs son sutiles, pero afectan a las conformaciones de los lazos en las crestas de unión al receptor (receptor-binding ridge en la figura). En ambas RBMs, uno de los lazos de la cresta contiene un enlace disulfuro que es crítico en la unión.
SARS-CoV y bat-CoV Rs3367 tienen un resto con tres residuos Pro-Pro-Ala en dicho lazo; pero en SARS-CoV-2 y bat-CoV RaTG13 muestran un motivo de cuatro residuos Gly-Val/Gln-Glu/Thr-Gly; así la conformación del bucle cambia gracias a que las glicinas son más flexibles.
Este cambio favorece la unión RBD/hACE2. Además, la hendidura hidrófoba que se forma tiene una conformación más compacta gracias a los puentes de hidrógeno Asn487 y Ala475 en SARS-CoV-2 RBM, con lo que el lazo que contiene Ala475 se coloca más cerca de hACE2.
La comparación con SARS-CoV RBM muestra que estos pequeños cambios estructurales de SARS-CoV-2 RBM son más favorables para la unión con hACE2.
Son diferencias escasas , pero desde el punto de vista funcional, decisivas.
Se han descrito dos puntos críticos de unión (virus-binding hotspots), el punto crítico hotspot-31 en el puente salino Lys31 y Glu35, y el hotspot-353 en otro puente salino entre Lys353 y Asp38.
Estos dos puentes salinos son débiles, debido a la gran distancia en la interacción, pero como están encerrados en un entorno hidrófugo, que reduce la constante dieléctrica efectiva, su energía de enlace es mayor.
¿Cómo ataca el COVID al organismo?
El nudo gordiano de éste ataque o anclaje del virus:la llamada proteína S ( spike protein) que es el sitio de unión o de anclaje ( dividido en dos subunidades; S1 encargada de la unión o anclaje del virus y la subunidad S2, encargada de la fusión).
Esta proteína S está en contínua rotación. Tiene dos estructuras dinámicas : up y down.
La proteasa de hACE/2 rompe la proteína S en dos y libera un epítopo proteico el cual permite la unión con la célula humana.
Dentro vídeo.
Para ello, la proteína S ha de estar en una determinada posición. Ver vídeo en la bitácora, con una posicion "up" y otra " down" .
Esta peculiar estructura de la proteína S hace que interrelacione con una proteasa que hace un "cleavage" o rotura de la misma mediante
a)Una proteasa de furina
b) Una proteína llamada TMPRSS2. ( Interfiriendo éste paso es donde se encuentra el mecanismo de acción de dos posibles antivirales, Camustat u Nafamustat.
Dicho en sencillo es así. El proceso parece ser bastante , muchísimo, mas complicado.
Sabemos igualmente que para que el COVID19 entre dentro de la célula epitelial del pulmón, su target o diana más adecuado, necesita de una proteasa furilo ( lo explicamos en otro artículo). Y sabemos que hay sustancias como el Mesilato de Camustat y el Nafamustat que actúan a ese nivel anulando la proteína TMPRSS.
Esta figura de arriba muestra la estructrura primaria. El genoma del COVID19 es de 29-32 kilobases, siendo una sola cadena de RNA que se replica en el sentido de las aGUJAS DEL RELOSJ Está el dominio terminal N (NTD) antecede al dominio de unión con el receptor (RBD) que incluye el motivo de unión con el receptor (RBM). Tras los subdominios SD1 y SD2, y el péptido de fusión (FP), aparecen las dos regiones de héptadas repetidas, HR1 y HR2.Se están probando fármacos que actúan sobre éstos dominios Hr1 y Hr2.
Finaliza la región transmembrana (TM) y el dominio intracelular (IC).
Etiquetas:
ACE/2,
Camustat,
COVID-19,
nafamustat,
RBD,
RBM,
SARS-CoV-2,
unión
lunes, 30 de marzo de 2020
Alfa ceto glutamidas (AKG) como posibles inhibidores de la proteasa del Coronavirus COVID-19.
Mírenlo bien: esta estructura es la proteína S del COVID19 y puede ser la molécula que nos permita encontrar un fármaco que pueda tratar al COVID19.
La actual pandemia del beta coronavirus de Wuhan ( COVID-19) está mediada por un virus RNA monocatenario, de tamaño 50-200 nanometros, con una serie de azúcares en la cubierta externa lo que le hace ser "relativamente pesado". Parece ser que la vida media del virus en aerosol es de 66 minutos, y que al cabod e las tres horas se deporita en el suelo. Esto es muy arreisgado y las declaraciones de una portavoz de la OMS , la Dra Maria van Kerkhouve diciendo que no hace falta mascarillas porque no es una transmisión "airborne" nos parecen UNA TEMERIDAD.
El virus COVIS-19 es MUY contagioso con una R0 = 2,7, muy superior a los ortomixovirus de la "gripe vulgar" que es de R0=1,3.
Aunque les cueste creerlo, se puede patentar la secuencia de ARN de un virus, que aunque parezca natural ( o no, y es una arma biolñógica) no deja de ser un sisnsentido patentarlo como si fuera un dentífrico. Los virus SARS y MERS fueron patentados, como atestigua:
https://patentimages.storage.googleapis.com/6b/c3/21/a62eb55a0e678c/US7220852.pdf y MERS-CoV (MERS) https://data.epo.org/publication-server/pdf-document?pn=2898067&ki=B1&cc=EP&pd=20200115
En sólamente dos meses el COVID-19 está siendo exhaustivamente estudiado: por la encuesta epidemiológica se supone que es infectante en la fase asintomática ( de 2 a 14 días, con una media de 5 días) y también en las dos semanas posteriores a la "curación· de la enfermedad.
En la superficie del virus nos encontramos las proteínas S ( con dos subunidades S1 y S2) , y la proteína M .
El ARN monocatenario del COVID-19 codifica la poliproteína
ORF1b que se escinde en varias proteínas relevantes en su replicación.
Una de ellas es la polimerasa de ARN dependiente de ARN, llamada RdRp, o nsp12, clave en la catálisis de la síntesis del ARN del virus y diana de fármacos antivirales como remdesivir y sofosbuvir.
Se acaba de publicar en bioRxiv la estructura tridimensional del complejo proteico nsp12-nsp7-nsp8; se ha obtenido por criomicroscopia electrónica (cryo-EM) con una resolución de 2.9 Å. Además de ayudar a entender cómo actúan remdesivir y sofosbuvir, se espera que permita desarrollar nuevos antivirales específicos
Yan Gao, Liming Yan, …, Zihe Rao, «Structure of RNA-dependent RNA polymerase from 2019-nCoV, a major antiviral drug target,» bioRxiv preprint (16 Mar 2020), doi: https://doi.org/10.1101/2020.03.16.993386. Seguro que se publicará en Nature Communications, como ya lo hizo el artículo sobre SARS-CoV, Robert N. Kirchdoerfer, Andrew B. Ward, «Structure of the SARS-CoV nsp12 polymerase bound to nsp7 and nsp8 co-factors,» Nature Communications 10: 2342 (28 May 2019), doi: https://doi.org/10.1038/s41467-019-10280-3.

La estructura 3D del complejo proteico nsp12-nsp7-nsp8 del coronavirus humano SARS-CoV se publicó en Nature Communications en 2019. Comparte muchas semejanzas (estructuras conservadas) con la de SARS-CoV-2 (antes llamado 2019-nCoV). Pero las pocas diferencias son claves para el desarrollo de antivirales específicos contra COVID-19. Esta figura muestra las diferencias entre las secuencias de aminoácidos de la proteína nsp12 del nuevo coronavirus humano SARS-CoV-2 (2019-nCoV en la figura), el coronavirus humano SARS-CoV y el coronavirus de murciélagos RaTG13. Parecen pocas diferencias, pero son suficientes para que los antivirales más eficaces contra SARS no sean los más eficaces contra COVID-19.
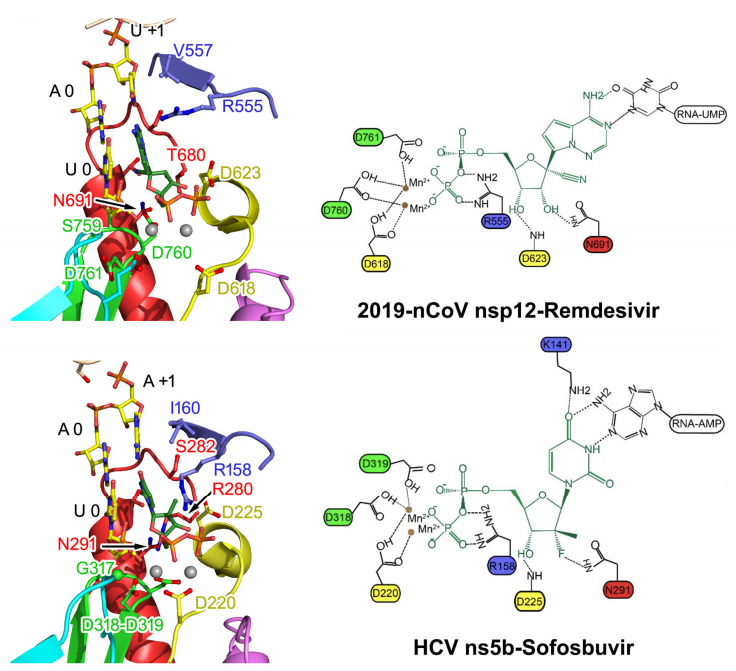
La estructura tridimensional a escala atómica de la proteína nsp12 permite estudiar con todo lujo de detalles su interacción con antivirales.
El fármaco que más posibilidades tiene de ser útil es el Remdesivir, del laboratorio americano Gilead, que se va a estudiar en el Ensayo Clínico "Solidaruty" de la OMS.s
Fuentes: (Manli Wang, Ruiyuan Cao, …, Gengfu Xiao, «Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro,» Cell Research 30: 269-271 (04 Feb 2020), doi: https://doi.org/10.1038/s41422-020-0282-0; Michelle L. Holshue, Chas DeBolt, …, Satish K. Pillai, «First Case of 2019 Novel Coronavirus in the United States,» The New England Journal of Medicine (NEJM) 382:929-936 (05 Mar 2020), doi: https://doi.org/10.1056/NEJMoa2001191).
y tres tipos de proteínas, la proteína Espikulada ( Spike proteín) ,que es tiene una estructura conformacional representada en el video que tienen abajo.
Esta proteína S está compuesta por dos subunidades , S1:encargada del ANCLAJE del virus;
y S2, que es la que se encarga de la FUSION y posterior introducción a la célula del pulmón, uniéndose al receptor ACE/2..
ésta proteína S ha sido secuenciada y su estructura está mostrada abajo:
formando parte del genoma del virus y tiene entre 1120 y 1200 kdalton.
En la zona de líneas discontínuas de abajo
Es la forma mediante la cual el virus se une a un receptor ACE/2 ( angiotensina y el receptor RBD del COVID-19.
Este receptor es más abundante en las células epiteliales de pulmón y , que vemos estructuralmente aquí abajo por microscopía crioelectrónica. Esta técnica fue premiada con el premio Nobeld e medicina, hace dos años.:
Si ampliamos un poco más la imagen , vemos como ése receptor va a ser menos abundante en niños, por debajod e 16 años, quizás por eso es por lo que hay menos casos en infantes. Al parecer sólo ha habido muy pcos casos y quizás ea porque en esas edades tempranas de la vida el sistema ACe/2 de la angiotensina está muy inmduro. Hay pocos niños afortunadamente con hipertensión renal por exceso de angiotensina.
O más aumentada la imagen:
Otra de las estrategias de ataque sería la presencia de una MPro, o proteasa que está igualmente en la superficie del virus y tiene ésta estructura:
Esta proteasa se ha visto que es inhibida por una serie de sustancias que se llaman AKG, inhibidores del alfa Ceto glutamida, que son pro fármacos activados por peróxidod e hidrógeno, con la estructura básica:
cuya estructura química tenemos abajo: son los compuestos experimentales 13 a,13 b y 11 r.
Estructura química de los inhibidores de la alfa cetoglutamida ( AKG) , denominados compuesto 11r, 13 a y 13 b.
Estas sustancias inhiben la proteasa del COVID-19.tal como queda reflejado en l a siguiente imagen, que es la unión específica al compuesto 13 b.:se produce un ataque nucleofílico de la cys en el grupo cetónico y se forma un tio hemi ketal, en reacción reversible, lo que se sabe por la densidad electrónica de ésta molécula quiral
El grupo oxidrilo de éste tio hemi ketal se estabiliza por enlaces de puentes de hidrógeno desde la cadena de amidas de los aminoácidos Cisteína y Glicina (y parcialmente serina)
el RESTO DE LA EXPLICACIÓN es un manual de química farmacéutica que es una delicia no truducir y leerlo directamente del ingles:
Compound 13b inhibits the purified recombinant 2019-nCoV Mpro with IC50 = 0.67 ± 0.18 μM. The corresponding IC50 values for inhibition of the SARS-CoV Mpro and the MERS-CoV Mpro are 0.9 ± 0.29 μM and 0.58 ± 0.22 μM, respectively. In a SARS-CoV replicon (Kusov et al., 2015), RNA replication is inhibited with EC50 = 1.75 ± 0.25 μM. In human Calu3 cells infected with MERS-CoV, the compound showed excellent antiviral activity (Lucie Sauerhering & Stephan Becker personal communication).
As the next steps in the development of compound 13b towards a potential drug targeting 2019-nCoV or other coronaviruses, we will undertake tests in virus-infected cell cultures and in a small-animal model (once it will become available for 2019-nCoV). Meanwhile, our crystal structures may be used by others for virtual screening and de-novo design of inhibitors.
Etiquetas:
algorritmo,
COVID-19,
estructura,
inhibidores;AKG,
tridimensional
Suscribirse a:
Comentarios (Atom)







































